Το Προφίλ Λιπαρών Οξέων
ως Εργαλείο Γονιμότητας
Πώς η εξατομικευμένη ανάλυση του λιπιδομικού προφίλ αίματος μπορεί να αλλάξει την κλινική προσέγγιση στη γονιμότητα, το IVF, το PCOS και την ανδρική υπογονιμότητα.
Περιεχόμενα
- Τι μετράει η ανάλυση λιπαρών οξέων
- Γιατί ο λόγος Ω6:Ω3 είναι κλειδί
- Λιπαρά οξέα & ποιότητα ωαρίων
- IVF — αποτελέσματα & εμφύτευση
- PCOS — ο ρόλος της φλεγμονής
- AMH — επιφύλαξη & ισορροπία
- Ανδρική συμμετοχή — σπέρμα & DNA
- Κλινικό πρωτόκολλο αξιολόγησης
- Θεραπευτικές παρεμβάσεις
- Σημειώσεις & Βιβλιογραφία
Τι αποκαλύπτει η ανάλυση λιπαρών οξέων
Η ξηρά κηλίδα αίματος (Dried Blood Spot — DBS) αποτελεί μια ελάχιστα επεμβατική, βαλιδαρισμένη κλινικά μέθοδο ποσοτικοποίησης 11 λιπαρών οξέων απευθείας στις κυτταρικές μεμβράνες των ερυθροκυττάρων. Σε αντίθεση με τις συνήθεις εξετάσεις λιπιδίων νηστείας, αυτή η ανάλυση αντικατοπτρίζει τη σωρευτική, πραγματική κατάσταση των τελευταίων 4 μηνών — ακριβώς ο κύκλος ζωής ενός ερυθροκυττάρου, αλλά και ο χρόνος ωρίμανσης ενός ωοκυττάρου (ωοθυλακιογένεση).
Η ανάλυση παράγει έξι κλινικά σχετικούς δείκτες:
| Δείκτης | Τι μετρά | Κλινική Σημασία για Γονιμότητα |
|---|---|---|
| Λόγος Ω6:Ω3 | AA / EPA (ιδανικό <3:1) | Δείκτης συστηματικής φλεγμονής |
| Omega-3 Index | EPA + DHA (%) | Ποιότητα κυτταρικής μεμβράνης ωοκυττάρων |
| AA Index | Arachidonic Acid (%) | Pro-inflammatory status — σχετίζεται με OHSS, PCOS |
| Cell Membrane Health | Ισορροπία κορεσμένων / πολυακόρεστων | Διαπερατότητα — απορρόφηση θρεπτικών στο ωοθυλάκιο |
| Cognitive FA Score | DHA / AA ratio | Νευρολογική ανάπτυξη εμβρύου (Q1) |
| Total FA Profile Score | Σύνθετη βαθμολογία | Συνολική εκτίμηση λιπιδομικής υγείας |
Η ωοθυλακιογένεση διαρκεί ~90–120 ημέρες. Το ωοκύτταρο που θα συλληφθεί στη διέγερση IVF άρχισε να ωριμάζει τρεις μήνες πριν. Συνεπώς, η ανάλυση DBS δίνει ακριβώς την κατάσταση του λιπιδικού μικροπεριβάλλοντος κατά την κρίσιμη αυτή φάση — κάτι που δεν επιτυγχάνεται από κανένα άλλο τυπικό εργαστηριακό τεστ.
Γιατί ο λόγος Ω6:Ω3 είναι τόσο σημαντικός
Ο εξελικτικά φυσιολογικός λόγος Ω6:Ω3 για τον ανθρώπινο οργανισμό εκτιμάται στο 1:1 έως 4:1. Η σύγχρονη Δυτική διατροφή — επεξεργασμένες τροφές, σπορέλαια (ηλιέλαιο, καλαμποκέλαιο), ελάχιστα λιπαρά ψάρια — έχει ανατρέψει δραστικά αυτή την ισορροπία.
στην Ευρώπη σήμερα
για πρώτη φορά είναι ελλειμματικά
για βέλτιστη κυτταρική λειτουργία
αποκατάσταση ισορροπίας
Το ανισορροπημένο λιπιδικό προφίλ δεν είναι απλά «κακή διατροφή». Στον αναπαραγωγικό άξονα, υψηλή AA (αραχιδονικό οξύ, Ω6) οδηγεί σε υπερπαραγωγή φλεγμονωδών προσταγλανδινών (PGE2, PGF2α), θρομβοξανών και λευκοτριενών — μορίων που παρεμβαίνουν άμεσα στην ωορρηξία, τη λειτουργία του ωχρού σωματίου, την εμφύτευση και τη διατήρηση της κύησης.
Πολλές γυναίκες παίρνουν ήδη omega-3 συμπληρώματα αλλά εξακολουθούν να εμφανίζουν δυσανάλογα υψηλό Ω6:Ω3, διότι (α) δεν έχουν μειώσει παράλληλα τη λήψη Ω6, (β) χρησιμοποιούν προϊόντα χαμηλής βιοδιαθεσιμότητας ή (γ) δεν έχουν επιτύχει επαρκή επίπεδα ιστού. Χωρίς μέτρηση, δεν γνωρίζουμε — εικάζουμε.

Λιπαρά οξέα και ποιότητα ωοκυττάρων
Το ωοθυλακικό υγρό (follicular fluid) αποτελεί το μικροπεριβάλλον του αναπτυσσόμενου ωοκυττάρου. Μελέτες φυγόκεντρησης ωοθυλακικού υγρού έχουν δείξει ότι η σύνθεσή του σε λιπαρά οξέα είναι στατιστικά συσχετισμένη με:
Υψηλότερα επίπεδα ALA συνδέονται με περισσότερα ώριμα MII ωοκύτταρα (p=0.005)
Αυξημένη πρόσληψη ALA & EPA: υψηλότερα ποσοστά γονιμοποίησης σε ICSI (p<0.003)
DHA αυξάνει τη ρευστότητα μεμβράνης — κρίσιμη για την ενεργειακή παραγωγή (ATP) του ωοκυττάρου
EPA/DHA μειώνουν οξειδωτικό στρες στο ωοθυλάκιο — παράγοντας ωοκυτταρικής γήρανσης
Omega-3 βελτιώνουν μικροκυκλοφορία — αυξημένη αιμάτωση ωοθηκών κατά τη διέγερση
Μελέτες σε ποντίκια: διά βίου διατροφή πλούσια σε Ω3 παρατείνει αναπαραγωγική λειτουργία και βελτιώνει ωοκυτταρική ποιότητα
αύξηση πιθανότητας κλινικής κύησης σε IVF για κάθε τεταρτημόριο αύξησης EPA+DHA στο αίμα — EARTH Cohort Study, Harvard T.H. Chan School of Public Health
Chiu et al. (2018), Human Reproduction. Μεγάλη κοόρτη (n>900 γυναίκες, >1.200 κύκλοι IVF). Πολυμεταβλητή ανάλυση ελεγμένη για BMI, ηλικία, αιτία υπογονιμότητας κ.λπ.
IVF & ICSI — Τι δείχνει η βιβλιογραφία
Η σχέση Ω3 λιπαρών οξέων με τα αποτελέσματα IVF είναι από τα πλέον τεκμηριωμένα πεδία. Παρακάτω συνοψίζονται τα ισχυρότερα ευρήματα:
| Παράμετρος IVF | Συσχέτιση με Ω3 | Ποιοτικό επίπεδο ενδείξεων |
|---|---|---|
| Αριθμός ωοκυττάρων MII | Θετική (ALA tertile 3 vs 1, p=0.005) | Μέτριο–Ισχυρό |
| Ποσοστό γονιμοποίησης | Θετική (EPA, p=0.003) | Μέτριο–Ισχυρό |
| Ποιότητα εμβρύου (μορφολογία) | Θετική (Hammiche et al., 2011) | Μέτριο |
| Ζωντανή γέννηση (live birth) | 54% vs 36% (Q4 vs Q1 EPA+DHA) | Ισχυρό (EARTH cohort) |
| Απώλεια κύησης | Αντίστροφη: 5% vs 53% (Q4 vs Q1) | Ισχυρό |
| Φυσική σύλληψη (κοόρτη) | ~2× πιθανότητα σύλληψης με Ω3 συμπλήρωμα | Μέτριο |
| Εμφύτευση / ενδομητρική δεκτικότητα | Θετική μέσω αντι-φλεγμονωδών προσταγλανδινών | Μέτριο (έμμεσες ενδείξεις) |
Η σχέση Ω3 → live birth φαίνεται να διαμεσολαβείται κυρίως από μείωση των αποβολών (pregnancy loss), όχι τόσο από αύξηση της γονιμοποίησης αυτής καθεαυτής. Αυτό υποδηλώνει ότι τα Ω3 παίζουν κρίσιμο ρόλο στη φάση εμφύτευσης και πρώιμης ανάπτυξης — πιθανώς μέσω ρύθμισης ενδομητρικού μικροπεριβάλλοντος και ανοσολογικής ανοχής (Th1/Th2 ισορροπία).
Η προκλινική έρευνα σε μυϊκά μοντέλα δείχνει επίσης ότι η ανεπάρκεια FADS2 (ενζύμου βιοσύνθεσης Ω3/Ω6) οδηγεί σε διαταραχή γοναδικών μεμβρανικών δομών και βλάπτει τόσο τη γυναικεία όσο και την ανδρική γονιμότητα — υποδηλώνοντας ότι η λιπιδική σύνθεση είναι, εκτός ηλικίας και BMI, θεμελιώδης ρυθμιστής αναπαραγωγικής λειτουργίας.
PCOS — Φλεγμονή, ινσουλίνη και λιπαρά οξέα
Το PCOS χαρακτηρίζεται από τριγωνική αλληλεπίδραση: χρόνια χαμηλόβαθμη φλεγμονή → αντίσταση στην ινσουλίνη → υπερανδρογοναιμία. Τα Ω6 λιπαρά οξέα, ιδίως το αραχιδονικό (AA), είναι πρόδρομοι pro-inflammatory προσταγλανδινών (PGE2) που ενεργοποιούν τον NF-κB — κεντρικό ρυθμιστή φλεγμονής.
Πώς Ω6 επιδεινώνει PCOS
- Αυξάνει IL-6, TNF-α, CRP — φλεγμονή
- Ενισχύει ινσουλινοαντίσταση μέσω ER stress
- Στρέφει LH/FSH προς ανδρογόνα
- Διαταράσσει ωοθυλακιογένεση → ανωοθυλακιορρηξία
- Αυξάνει AMH (βλ. επόμενη ενότητα)
Πώς Ω3 αντιτίθεται στο PCOS
- Μειώνει CRP, IL-6, MDA μέσω PPAR-α/γ
- Βελτιώνει ευαισθησία ινσουλίνης (IRS-1 pathway)
- Μειώνει τεστοστερόνη ορού
- Αποκαθιστά εμμηνορρυσιακή κανονικότητα
- Βελτιώνει λιπιδαιμικό προφίλ (TG: −29 mg/dL)
γυναίκες με PCOS ανέφεραν κανονική εμμηνορρυσία μετά από 8 εβδομάδες λήψης 3g Ω3/ημέρα, έναντι μόνο 22.9% στην ομάδα placebo — Nadjarzadeh et al., RCT
Μια μετα-ανάλυση (2016) δεν βρήκε στατιστικά σημαντική επίδραση στην ινσουλινοαντίσταση (HOMA-IR) σε σχετικά μικρές RCTs. Ωστόσο, νεότερη μετα-ανάλυση 9 RCTs (n=591) έδειξε σημαντική μείωση HOMA-IR, χοληστερόλης και τριγλυκεριδίων. Η διαφορά αποδίδεται σε δοσολογία (>2g/ημέρα EPA+DHA), διάρκεια (>8 εβδομάδες) και τύπο PCOS.
Για κλινικούς, η αξία της μέτρησης λιπαρών οξέων στο PCOS είναι διπλή: (α) αξιολογεί το φλεγμονώδες φορτίο αντικειμενικά και (β) επιτρέπει παρακολούθηση ανταπόκρισης σε διατροφικές παρεμβάσεις, αποτελώντας συμπληρωματικό βιοδείκτη πέραν του BMI και των κλασικών ορμονικών παραμέτρων.
AMH — Ισορροπία, PCOS και λιπαρά οξέα
Η Anti-Müllerian Hormone (AMH) αποτελεί τον βασικό βιοδείκτη ωοθηκικής επιφύλαξης (ovarian reserve). Η ερμηνεία της πρέπει να γίνεται πάντα στο πλαίσιο του συνολικού προφίλ:
| Σενάριο AMH | Πιθανή Αιτία | Λιπαρά Οξέα — Σχέση |
|---|---|---|
| Χαμηλό AMH (<1.0 ng/mL) | Μειωμένη επιφύλαξη, ηλικία, χημειοθεραπεία | DHA/EPA προστατεύουν ωοκύτταρα — antiapoptotic δράση σε κοκκιώδη κύτταρα |
| Υψηλό AMH + PCOS (>6.0 ng/mL) | Ανωοθυλακιορρηξία, follicular arrest | Ω3 μειώνουν ινσουλινοαντίσταση → έμμεση ρύθμιση AMH |
| Φυσιολογικό AMH + Αποτυχία IVF | Ωοκυτταρική ποιότητα, μιτοχονδριακή δυσλειτουργία | Ω3 index κρίσιμος — ποιότητα μεμβράνης ανεξάρτητη από ποσότητα |
Το AMH μετρά ποσότητα ωοθυλακίων. Τα λιπαρά οξέα στοχεύουν ποιότητα ωοκυττάρων. Και τα δύο έχουν ανεξάρτητη προγνωστική αξία. Γυναίκες με καλό AMH αλλά κακό λιπιδικό προφίλ μπορεί να έχουν πολλά ωοκύτταρα χαμηλής ποιότητας — και αντιστρόφως.
Η λεπτομερής λιπιδική ανάλυση αποκτά επιπλέον αξία σε γυναίκες με χαμηλή ωοθηκική επιφύλαξη (DOR), όπου η βελτίωση της ποιότητας του κάθε διαθέσιμου ωοκυττάρου είναι κρίσιμη.
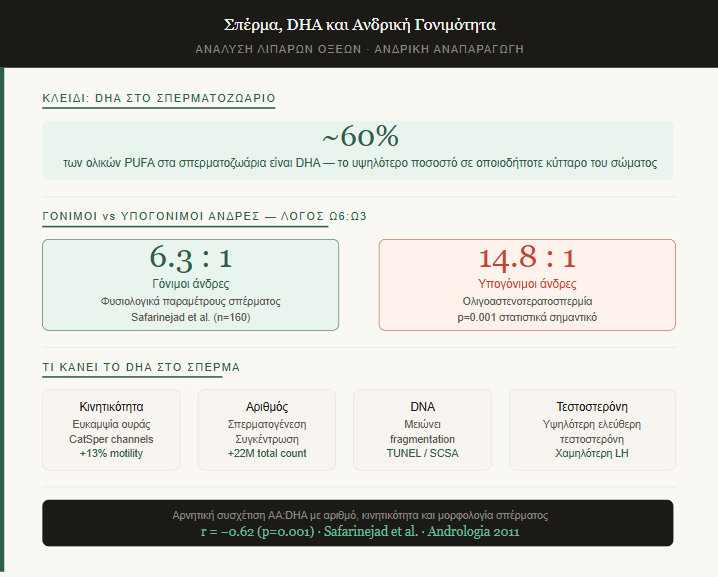
Σπέρμα, DHA και ο λόγος Ω6:Ω3
Το σπερματοζωάριο είναι ένα κύτταρο εξαιρετικά εξαρτημένο από τη σύνθεση λιπαρών οξέων της μεμβράνης του. Το DHA αποτελεί ~60% των ολικών PUFA στα σπερματοζωάρια — ένα μοναδικό χαρακτηριστικό που συνδέεται άμεσα με κινητικότητα και ικανότητα γονιμοποίησης.
DHA αυξάνει ευκαμψία ουράς — απαραίτητη για υπερενεργοποιημένη κινητικότητα (CatSper channels) προς ωάριο
Ω3 συμπλήρωμα: +22M total count, +13 M/mL συγκέντρωση σε ολιγοαστενοτερατόσπερμους άνδρες (p=0.001)
Επαρκή Ω3 → ακέραια ακρωσωμιακή αντίδραση και δομή κεφαλής σπερματοζωαρίου
Ω6/Ω3 υψηλός: αυξημένη λιπιδική υπεροξείδωση → DNA fragmentation (TUNEL+, SCSA+)
EPA/DHA: θετικά συσχετισμένα με SOD, catalase δραστηριότητα — αντιοξειδωτική θωράκιση σπέρματος
Fish oil (DHA) → υψηλότερη ελεύθερη τεστοστερόνη, μεγαλύτερος όγκος όρχεων, χαμηλότερη LH
Σε μελέτη ανδρών (n=160, Safarinejad et al.), ο λόγος Ω6/Ω3 ήταν 14.8±4.3 στους υπογόνιμους έναντι 6.3±2.2 στους γόνιμους (p=0.001). Το AA:DHA και AA:EPA είχαν ισχυρή αρνητική συσχέτιση με συνολικό αριθμό σπέρματος, κινητικότητα και μορφολογία (r ≈ −0.62).
Σε ζεύγη που υποβάλλονται σε ICSI λόγω ανδρικού παράγοντα, η αξιολόγηση και βελτίωση του λιπιδικού προφίλ του άνδρα αποτελεί επιπλέον — και πολλές φορές αναξιοποίητο — σημείο θεραπευτικής παρέμβασης.
Η βιβλιογραφία υποστηρίζει αξιολόγηση και των δύο μελών του ζεύγους. Μελέτη EARTH (Gaskins et al.) σε 229 ζεύγη (410 κύκλοι ART) έδειξε ότι η EPA+DHA πρόσληψη της γυναίκας σχετίζεται με ζωντανή γέννηση, ενώ η ALA πρόσληψη του άνδρα σχετίζεται με αριθμό και κινητικότητα σπέρματος. Αμφότερα λειτουργούν ανεξάρτητα — και αθροιστικά.
Πρωτόκολλο αξιολόγησης για κλινικούς
Σημείωση: Το πρωτόκολλο βασίζεται σε συνθετική ανάλυση της βιβλιογραφίας και δεν αποτελεί επίσημη κλινική οδηγία. Απαιτείται ιατρική παρακολούθηση.
Από τα αποτελέσματα στη δράση
Διατροφικές Πηγές Ω3
- Σαρδέλες, αντσούγιες, σκουμπρί (EPA+DHA)
- Σολωμός άγριας αλίευσης (>2g Ω3/μερίδα)
- Ρέγκα, τσιπούρα, γαρίδες
- Καρύδια (ALA — 2.5g/χούφτα)
- Σπόροι chia, λιναρόσπορος (ALA)
- Φύκια / microalgae oil (DHA — vegan)
Μείωση Ω6 — Το “Άλλο Μισό”
- Αντικατάσταση ηλιελαίου με ελαιόλαδο
- Μείωση επεξεργασμένων τροφίμων
- Αποφυγή καλαμποκελαίου, σογιελαίου
- Επιλογή ζωικών τροφίμων από βοσκότοπους (grass-fed)
- Περιορισμός fast food και margarines
- Έλεγχος ετικετών — “hydrogenated oils”
Ένα επαρκές συμπλήρωμα Ω3 για γονιμότητα πρέπει να προσφέρει τουλάχιστον 1.000–2.000 mg EPA+DHA/ημέρα σε βιοδιαθέσιμη μορφή (triglyceride > ethyl ester), να συνοδεύεται από βιταμίνη D3 και αντιοξειδωτικά για τη σταθερότητα των PUFA. Η ταυτόχρονη μέτρηση επιβεβαιώνει ότι το συμπλήρωμα πραγματικά αλλάζει το προφίλ.
Συνδυαστικές παρεμβάσεις δείχνουν ιδιαίτερα υποσχόμενα αποτελέσματα. Σε PCOS, η τριάδα Ω3 + Myo-inositol + βιταμίνη D καλύπτει τρεις διαφορετικούς παθοφυσιολογικούς άξονες (φλεγμονή, ινσουλινοαντίσταση, ωορρηξία). Για ανδρική υπογονιμότητα, ο συνδυασμός DHA + βιταμίνη E δείχνει συνεργιστική δράση στη μορφολογία και κινητικότητα σπέρματος.
Τα πολυακόρεστα λιπαρά οξέα (PUFA), ιδίως EPA και DHA, είναι από τη φύση τους εξαιρετικά ευάλωτα στη λιπιδική υπεροξείδωση — ακριβώς λόγω των πολλαπλών διπλών δεσμών τους. Όταν οξειδωθούν πριν ενσωματωθούν στις κυτταρικές μεμβράνες, όχι μόνο χάνουν τη βιολογική τους δράση αλλά γίνονται ενεργά επιβλαβείς — παράγοντας αλδεΰδες και ελεύθερες ρίζες που επιδεινώνουν το οξειδωτικό στρες στο ωοθυλάκιο, στο ενδομήτριο και στο σπερματοζωάριο.
Τα συμπληρώματα Ω3 που συνδυάζονται με εκχύλισμα πολυφαινολών εξαιρετικού παρθένου ελαιολάδου (ιδανικά >750 mg/kg περιεκτικότητα — π.χ. ελευρωπαΐνη, υδροξυτυροσόλη) προσφέρουν ενσωματωμένη αντιοξειδωτική ασπίδα: προστατεύουν τα λιπίδια αίματος από οξείδωση κατά τη μεταφορά τους στους ιστούς. Η υδροξυτυροσόλη αναγνωρίζεται από την EFSA με εγκεκριμένο health claim για προστασία λιπιδίων αίματος από οξειδωτικό στρες (Reg. EC 432/2012).
Στο πλαίσιο της αναπαραγωγικής ιατρικής, αυτό σημαίνει ότι το DHA και το EPA φτάνουν στα ωοκύτταρα, στο ενδομήτριο και στα σπερματοζωάρια σε μη οξειδωμένη, βιολογικά ενεργή μορφή — διαφορά κλινικά σημαντική ιδιαίτερα σε γυναίκες με αυξημένο οξειδωτικό φορτίο (PCOS, ηλικία >35, χαμηλή επιφύλαξη) και άνδρες με παθολογικό σπέρμα.
Επιλεγμένη Βιβλιογραφία
- Chiu YH et al. (2018). Serum omega-3 fatty acids and IVF outcomes. Human Reproduction. EARTH Study Cohort.
- Gaskins AJ, Chavarro JE et al. (2022). Women’s and men’s intake of omega-3 fatty acids and ART outcomes. Am J Obstet Gynecol. PMC9308672.
- Stanhiser J et al. (2022). Omega-3 fatty acid supplementation and fecundability. Human Reproduction. PMC9308390.
- Hammiche F et al. (2011). Increased preconception omega-3 PUFA intake improves embryo morphology. Fertil Steril.
- Safarinejad MR et al. (2011). Omega-3 supplementation in idiopathic oligoasthenoteratospermia. Andrologia.
- Yuan M et al. (2021). Omega-3 PUFA on hormones, oxidative stress and inflammation in PCOS. Ann Palliative Med.
- Frontiers in Nutrition (2022). Omega-3 fatty acids and insulin resistance in PCOS. PMC9581053.
- Falsig AL et al. (2019). Omega-3 fatty acids on semen quality markers: PRISMA review. Andrology.
- Lipids in Health and Disease (2025). Global omega-3 status — >590,000 DBS samples. Torrissen et al.
- EJOG (2022). Omega-3 dietary intake for oocyte quality in ART: systematic review.
- PMC (2024). Effect of omega-3 supplements or diets on fertility in women. PMC11019195.
- Nadjarzadeh A et al. (2015). Omega-3 on testosterone and menstrual cycle in PCOS. Iran J Reprod Med.
- EFSA (2012). Olive oil polyphenols — protection of LDL from oxidative stress. Reg. EC 432/2012.
